Innehåll
Molmassa, även känd som molekylmassa, är vikten på en mol av vilken kemisk förening som helst. En vanlig process inom kemi är att få den molära massan av kemiska föreningar för att blanda dem ordentligt. Med den periodiska tabellen och några enkla beräkningar kan du snabbt få den molära massan för vilken kemisk förening som helst, inklusive KCl, även känd som kaliumklorid. När du väl vet hur man får molmassan för KCl kan du enkelt använda samma teknik för att beräkna molmassan för vilken kemikalie som helst.
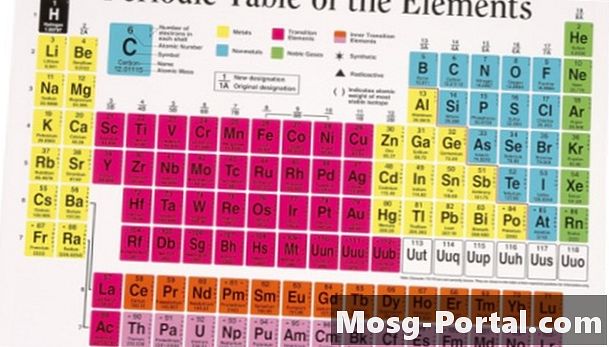
Slå upp kemikalien "K (kalium)" och kemikalien "Cl (klor) i den periodiska tabellen (se resurser). Skriv ner atommassan för både kalium och klor. För kalium är atommassan 35.453 och atom massan för klor är 39,0983.
Identifiera antalet atomer i den kemiska föreningen. Till exempel i KCl finns det bara en atom i var och en av de två kemikalierna. Du kan identifiera om det finns mer än en atom om det finns ett abonnemang skrivet under varje kemisk symbol. Om inget abonnemang skrivs, finns det bara en atom.
Beräkna för molmassa. Multiplicera antalet atomer för varje kemikalie multiplicerat med atommassan. Lägg till resultaten från att multiplicera siffrorna för att få den molära massan för föreningen. Till exempel för KCl (1 atom X 39,0983 kalium) + (1 atom X 35,453 klor) = (74,5513 g / mol) som är den molära massan för KCl.